Неорганическая цепочка (Натрий)
Не могу написать 4 уравнение, в третьем уравнение как бы не указана температура, значит не расплав, скорее всего раствор и получается соль тетрагидроксоалюминат натрия. А что дальше делать, я не знаю....
Приложения:
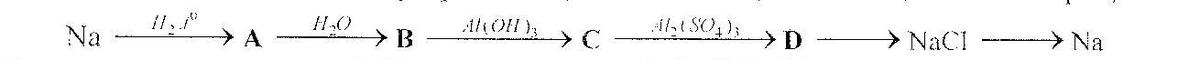
3) NaOH + Al(OH)3 = Na[Al(OH)4] (тетрагидроксоалюминат натрия) (реакция обмена)
Ответы
Ответ дал:
1
1) 2Na + H₂ = 2NaH (условие: t°C)
2) NaH + H₂O = NaOH + H₂↑
3) NaOH + Al(OH)₃ = Na[Al(OH)₄]
4) 6Na[Al(OH)₄] + Al₂(SO₄)₃ = 8Al(OH)₃↓ + 3Na₂SO₄
5) Na₂SO₄ + BaCl₂ = 2NaCl + BaSO₄↓
6) NaCl + K = KCl + Na (более активный металл вытесняет более слабый из его соли)
или
2NaCl (расплав) ---> 2Na + Cl₂ ( электролиз)
2) NaH + H₂O = NaOH + H₂↑
3) NaOH + Al(OH)₃ = Na[Al(OH)₄]
4) 6Na[Al(OH)₄] + Al₂(SO₄)₃ = 8Al(OH)₃↓ + 3Na₂SO₄
5) Na₂SO₄ + BaCl₂ = 2NaCl + BaSO₄↓
6) NaCl + K = KCl + Na (более активный металл вытесняет более слабый из его соли)
или
2NaCl (расплав) ---> 2Na + Cl₂ ( электролиз)
Спасибо большое за помощь. А как писать похожие реакции, как 4? Как догадаться продукты, и как расставить коэффициенты?
Вернее коэффициенты балансом можно
А продукты?
В интернете ни сова, о такой реакции))))
Логично, что С это соль - сульфат натрия ( так как дальше идёт соль- хлорид натрия)
А так как в реакции должен быть осадок, газ или вода, то ещё один продукт - гидроксид алюминия
А так как в реакции должен быть осадок, газ или вода, то ещё один продукт - гидроксид алюминия
Но, по идеи реакция обмена должна была обменяться частями?
Аналогичные реакции:
2K3[Cr(OH)6] + Fe2(SO4)3 = 2Fe(OH)3 + 2Cr(OH)3 + 3K2SO4
K3[Cr(OH)6] + 3SO2 = Cr(OH)3 + 3KHSO3
2K3[Cr(OH)6] + 3H2O2 = 2K2CrO4 + 2KOH + 8H2O
K3[Al(OH)6] + AlBr3 =2Al(OH)3 + 3KBr
2K3[Cr(OH)6] + Fe2(SO4)3 = 2Fe(OH)3 + 2Cr(OH)3 + 3K2SO4
K3[Cr(OH)6] + 3SO2 = Cr(OH)3 + 3KHSO3
2K3[Cr(OH)6] + 3H2O2 = 2K2CrO4 + 2KOH + 8H2O
K3[Al(OH)6] + AlBr3 =2Al(OH)3 + 3KBr
Я бы думал, что это связано с гидролизом солей. В растворе тетрагидроксоалюмината натрия среда сильнощелочная, а в растворе сульфата алюминия - кислая. Потому комплекс разрушается с выпадением осадка.
Спасибо большое за пояснения :)
Ответ дал:
1
Похожие вопросы
1 год назад
2 года назад
7 лет назад
7 лет назад
8 лет назад
2) NaH+H2O=NaOH + H2 - гидроксид натрия (реакция обмена