Ответы
Ответ дал:
0
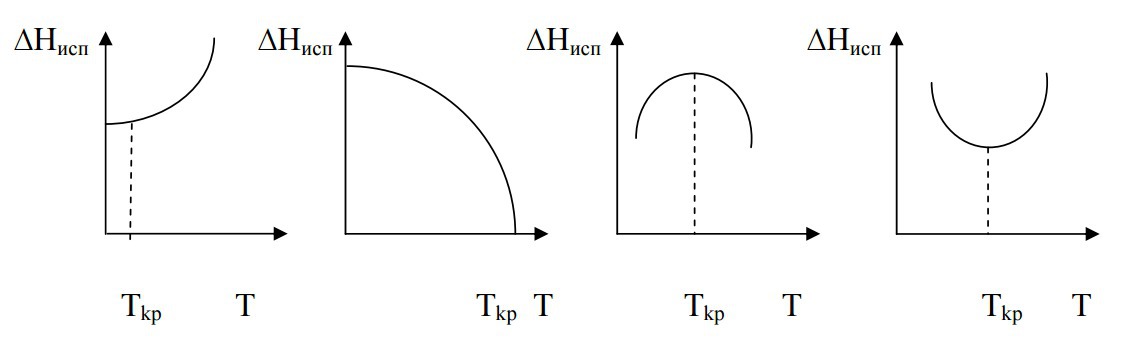
Если я правильно понимаю и помню, то правильный второй график, где ΔHисп уходит в нуль с ростом Т. Дело в том, что при температурах выше критической нет разницы между жидкостью и паром (газом). А значит, теплота переход (теплота испарения, теплота парообразования ΔH) должна быть равной нулю. Иначе был бы парадокс - пар и жидкость неотличимы, а для перехода нужна энергия - то есть разница все-таки есть.
Ответ дал:
0
Есть и другое определение - выше критической температуры пар никаким повышением давления невозможно превратить в жидкость. Значит, фазового перехода нет, значит и теплоты фазового перехода нет. Иначе говоря, она равна нулю
Похожие вопросы
2 года назад
2 года назад
7 лет назад
7 лет назад
9 лет назад
10 лет назад