Напишите уравнение реакции взаимодействия цинка с кислородом, укажите её тип. Вычислите массу цинковой пыли, которую нужно сжечь, чтобы получить 1000г оксида цинка.
Ответы
Ответ дал:
0
Ответ:
ответ смотри во вложении
Приложения:
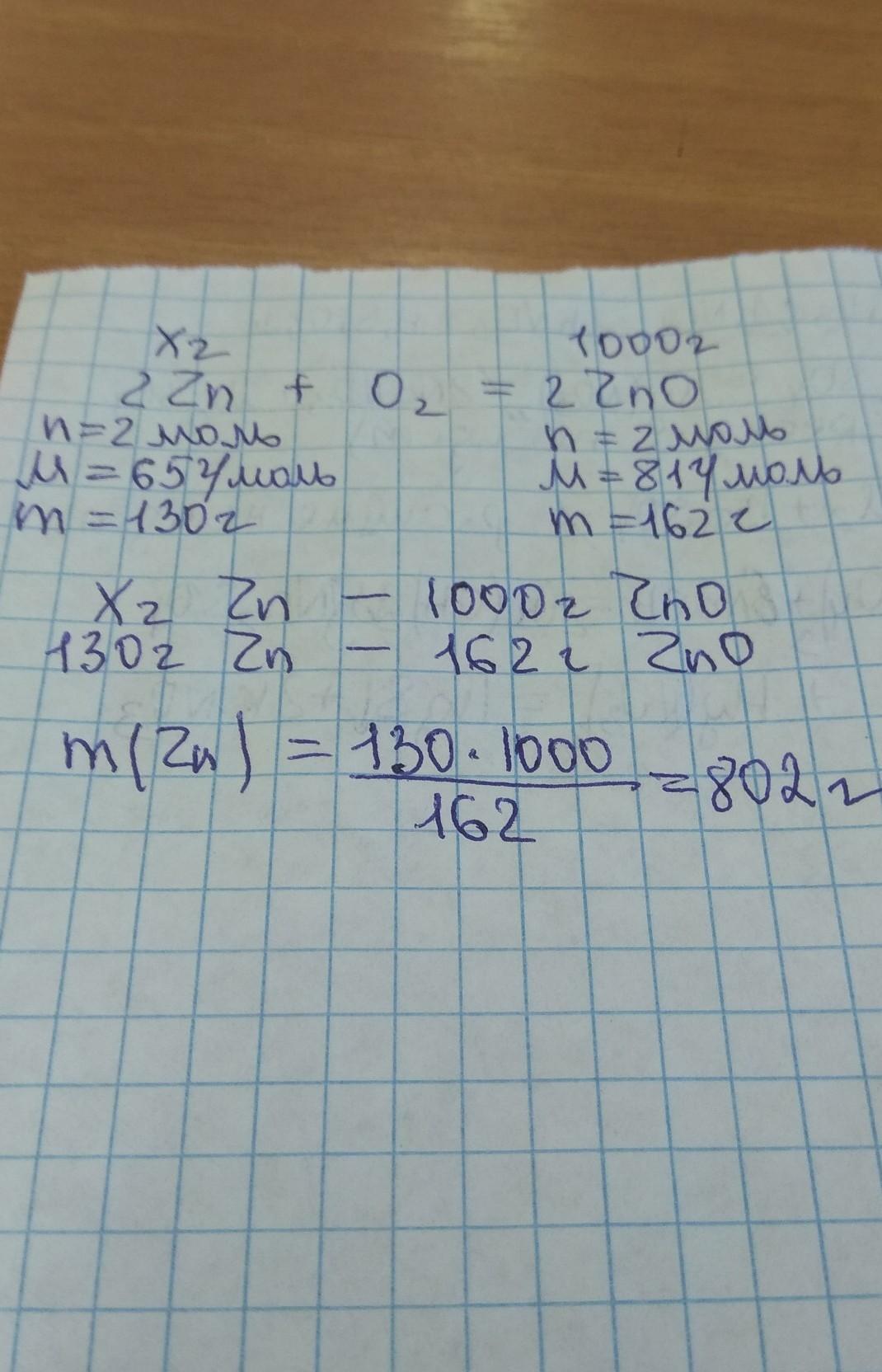
Ответ дал:
0
Ответ:
дано
m(ZnO) = 1000 g
-------------------
m(Zn) - ?
2Zn+O2-->2ZnO тип р-ции соединение
M(ZnO) = 81 g/mol
n(ZnO) = m/M = 1000 / 81 = 12.35 mol
2n(Zn) = 2n(ZnO) = 12.35 mol
M(Zn) = 65 g/mol
m(Zn) = n*M = 12.35 * 65 = 802.75 g
ответ 802.75г
Объяснение:
Приложения:
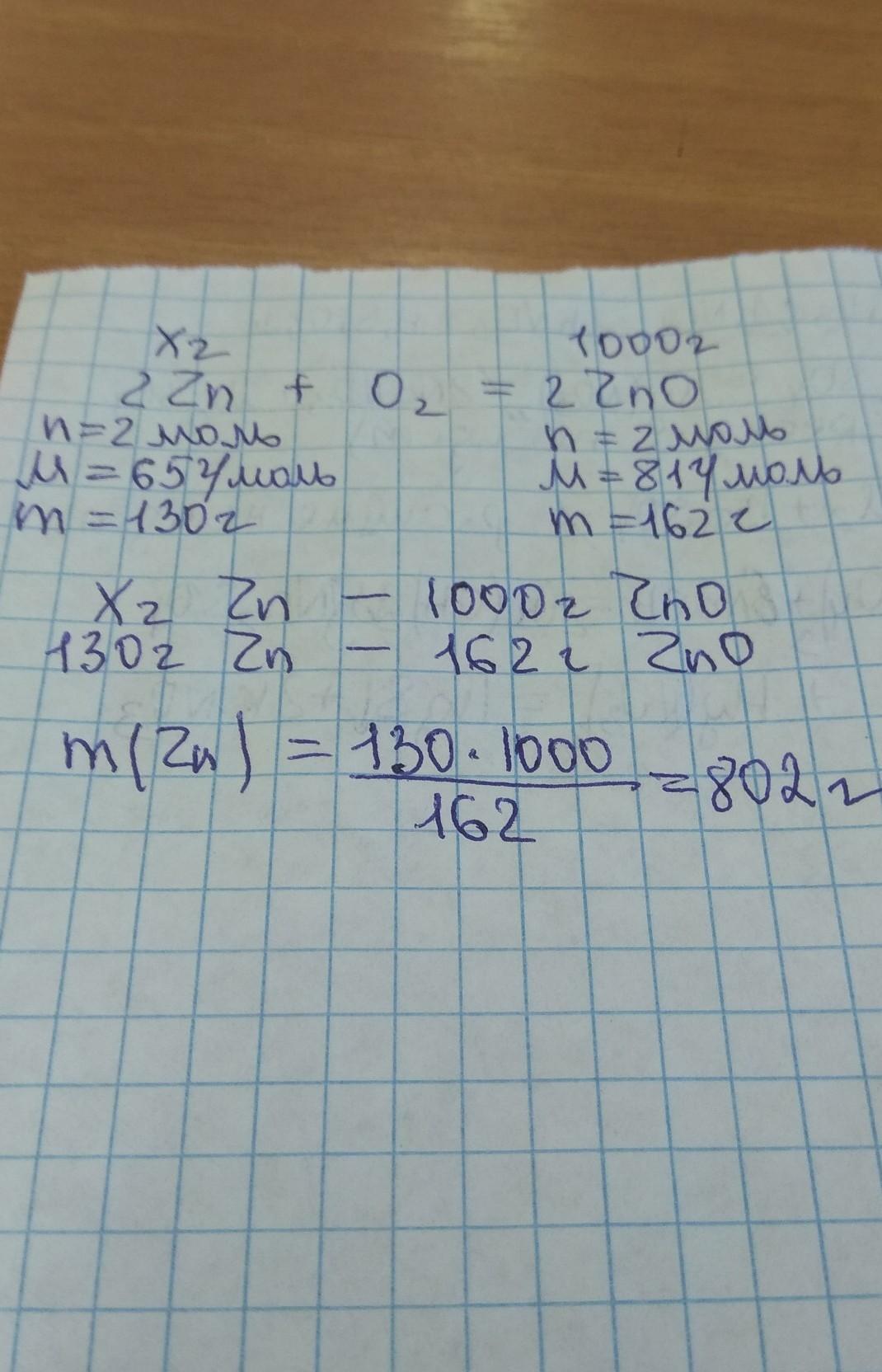
Похожие вопросы
2 года назад
2 года назад
2 года назад
8 лет назад
8 лет назад
9 лет назад