какие из приведенных реакции могут самопроизвольно протекать в нейтральном водном растворе?
Приложения:
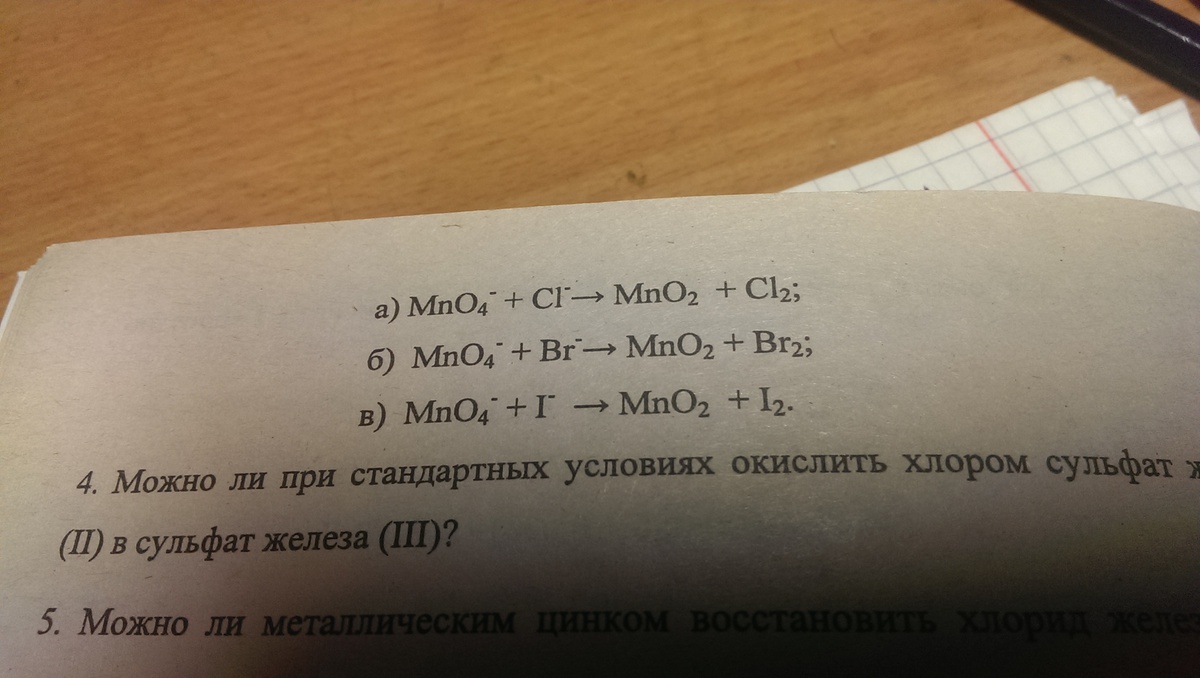
Ответы
Ответ дал:
0
1. Рассчитаем потенциал системы MnO4-/MnO2 при рН=7:
Е=1,69-0,059*рН*4/3=1,14 В
2. ECL/Cl-=1,358B
EBr2/Br-=1,087 B
EI2/I-=0,535 B
самопроизвольно пойдут те реакции, в которых потенциал окислителя (MnO4-) больше потенциала восстановителя(галогенид-ионы)
2. Это реакции между перманганатом и бромидом, перманганатом и иодидом
Е=1,69-0,059*рН*4/3=1,14 В
2. ECL/Cl-=1,358B
EBr2/Br-=1,087 B
EI2/I-=0,535 B
самопроизвольно пойдут те реакции, в которых потенциал окислителя (MnO4-) больше потенциала восстановителя(галогенид-ионы)
2. Это реакции между перманганатом и бромидом, перманганатом и иодидом
Похожие вопросы
2 года назад
2 года назад
7 лет назад
7 лет назад
10 лет назад
10 лет назад
10 лет назад